9月5日,我院腎臟病團隊在《科學(xué)(Science)》重要子刊《科學(xué)-免疫學(xué) (Science Immunology) 》發(fā)表了題為《METTL1介導(dǎo)Sarm1 mRNA發(fā)生m7G甲基化促進巨噬細胞炎癥反應(yīng)和多器官損傷(METTL1-mediated m7G methylation of Sarm1 mRNA promotes macrophage inflammatory responses and multiple organ injury)》的研究論文。藥學(xué)科學(xué)學(xué)院孟曉明教授和沈玉先教授為本文的通訊作者。博士后侯超、博士研究生張心茹、博士后衛(wèi)潔、青年教師汪佳男和安徽理工大學(xué)教授高健為本文的共同第一作者。
巨噬細胞因其表型與功能的高度可塑性,在炎癥發(fā)生和發(fā)展過程中扮演關(guān)鍵角色,但其調(diào)控的核心機制尚未被完全闡明。N7-甲基鳥苷(m7G)是一種由甲基轉(zhuǎn)移酶1(METTL1)等介導(dǎo)的高度保守的RNA修飾形式,對維持mRNA穩(wěn)定性及促進翻譯具有重要功能。然而,m7G修飾在炎癥及其關(guān)鍵效應(yīng)細胞——巨噬細胞中的功能及分子機制尚未見報道。
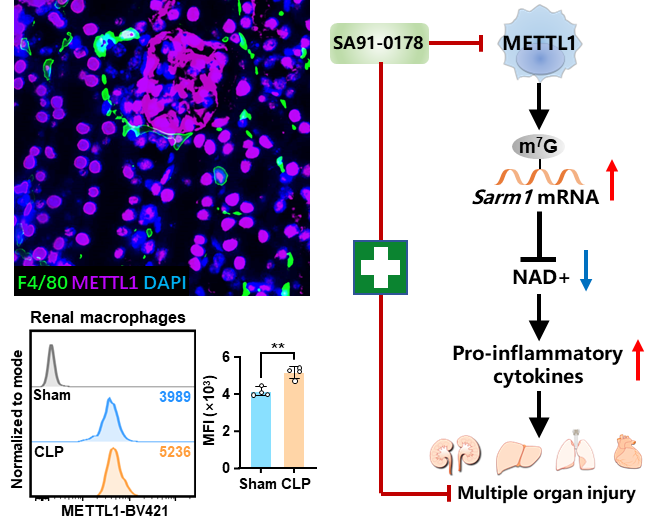
該研究系統(tǒng)揭示了mRNA m7G修飾的促炎效應(yīng)及其分子機制。研究發(fā)現(xiàn),在急性炎癥狀態(tài)下,巨噬細胞內(nèi)METTL1的表達及其介導(dǎo)的m7G修飾水平顯著上升,這一變化增強了Sarm1 mRNA的穩(wěn)定性,導(dǎo)致SARM1蛋白積累。作為經(jīng)典的NAD+水解酶,SARM1的積累進一步引起巨噬細胞內(nèi)NAD+的耗竭,從而驅(qū)動代謝重編程和炎性轉(zhuǎn)化,最終加劇急性炎癥及多器官損傷。此外,研究還篩選并驗證了新型METTL1酶活性抑制劑的抗炎效果,為臨床治療急性炎癥性疾病提供了新的策略和候選化合物。
該研究涉及的實驗均在安徽醫(yī)科大學(xué)平臺獨立完成,研究受到國家重點研發(fā)計劃、國家自然科學(xué)基金、國家資助博士后研究人員計劃等項目的資助。(藥學(xué)科學(xué)學(xué)院)
論文鏈接:https://www.science.org/doi/10.1126/sciimmunol.adv4810

 秉承“修身至善、博學(xué)悟真、中西兼容、知行并進”育人理念,培養(yǎng)“懂醫(yī)精藥、善研善成”高層次藥學(xué)專業(yè)人才。
秉承“修身至善、博學(xué)悟真、中西兼容、知行并進”育人理念,培養(yǎng)“懂醫(yī)精藥、善研善成”高層次藥學(xué)專業(yè)人才。 秉承“修身至善、博學(xué)悟真、中西兼容、知行并進”育人理念,培養(yǎng)“懂醫(yī)精藥、善研善成”高層次藥學(xué)專業(yè)人才。
秉承“修身至善、博學(xué)悟真、中西兼容、知行并進”育人理念,培養(yǎng)“懂醫(yī)精藥、善研善成”高層次藥學(xué)專業(yè)人才。 秉承“修身至善、博學(xué)悟真、中西兼容、知行并進”育人理念,培養(yǎng)“懂醫(yī)精藥、善研善成”高層次藥學(xué)專業(yè)人才。
秉承“修身至善、博學(xué)悟真、中西兼容、知行并進”育人理念,培養(yǎng)“懂醫(yī)精藥、善研善成”高層次藥學(xué)專業(yè)人才。 秉承“修身至善、博學(xué)悟真、中西兼容、知行并進”育人理念,培養(yǎng)“懂醫(yī)精藥、善研善成”高層次藥學(xué)專業(yè)人才。
秉承“修身至善、博學(xué)悟真、中西兼容、知行并進”育人理念,培養(yǎng)“懂醫(yī)精藥、善研善成”高層次藥學(xué)專業(yè)人才。









